- ปี พ.ศ.2549 กรมควบคุมโรค ได้มีคำสั่งแต่งตั้งคณะกรรมการจริยธรรมการวิจัย กรมควบคุมโรค ทำหน้าที่พิจารณาให้ความเห็นชอบเชิงจริยธรรมแก่โครงการวิจัย เพื่อให้การดำเนินงานวิจัยที่เกี่ยวข้องกับมนุษย์ เป็นไปตามหลักสากลและสอดคล้องตามหลักจริยธรรมการวิจัยในคน อันเป็นหลักประกันการคุ้มครองศักดิ์ศรี สิทธิ ความปลอดภัย และความเป็นอยู่ที่ดีของอาสาสมัคร
- ปี พ.ศ. 2565 ได้มีคำสั่งแต่งตั้ง คณะกรรมการจริยธรรมการวิจัยที่ไม่ได้ดำเนินการในมนุษย์ กรมควบคุมโรค โดยมี นายแพทย์สมเกียรติ ศิริรัตนพฤกษ์ เป็นประธาน เนื่องจากในการดำเนินงาน ที่ผ่านมาการติดตามการดำเนินงานของโครงการวิจัยที่ไม่ได้ดำเนินการในมนุษย์ยังไม่มีระบบการดำเนินงาน ที่ชัดเจน ทำให้ภายหลังจากที่โครงการวิจัยได้รับการอนุมัติรับรองไปแล้ว ไม่มีกระบวนการในการติดตามการดำเนินงาน
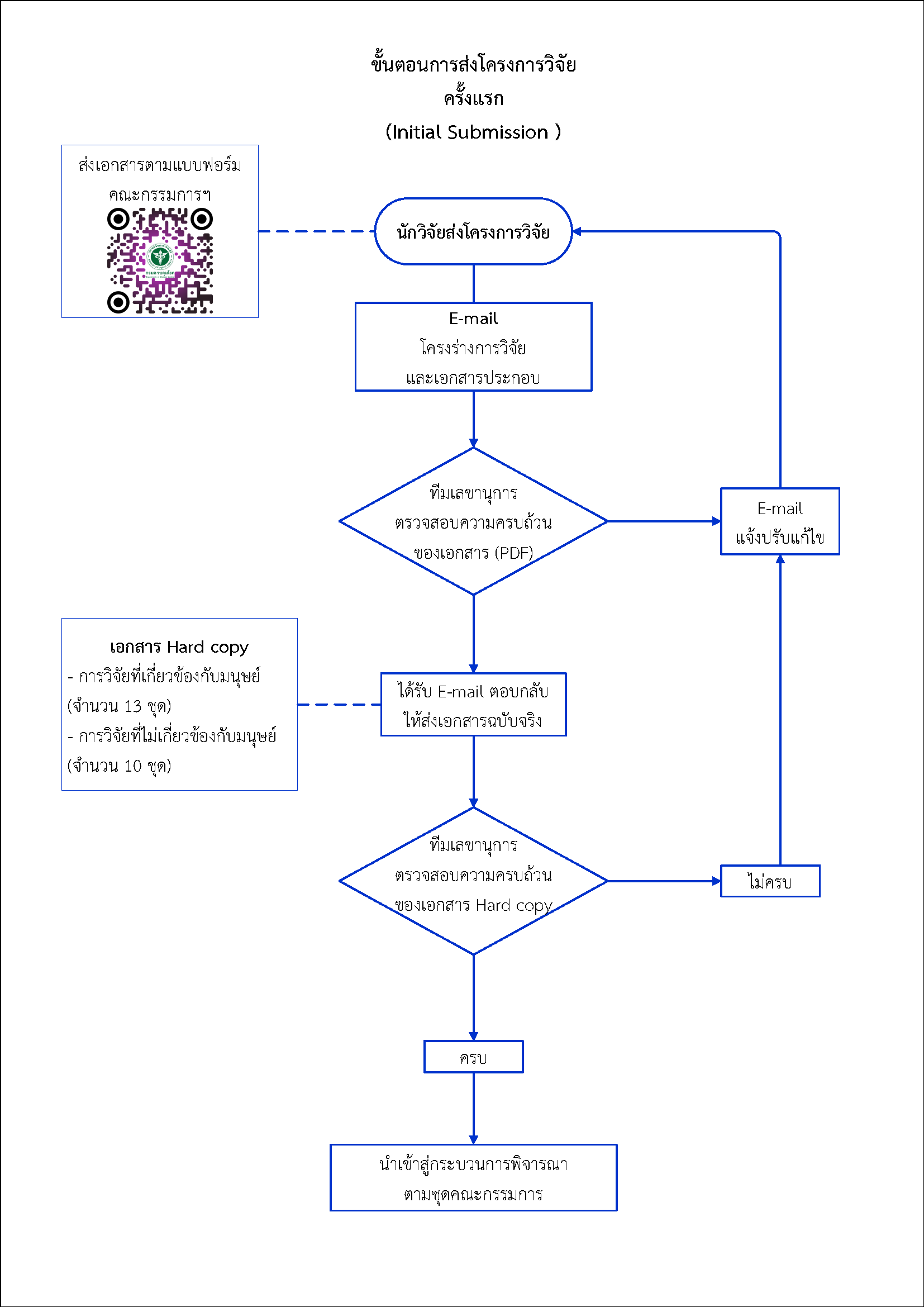
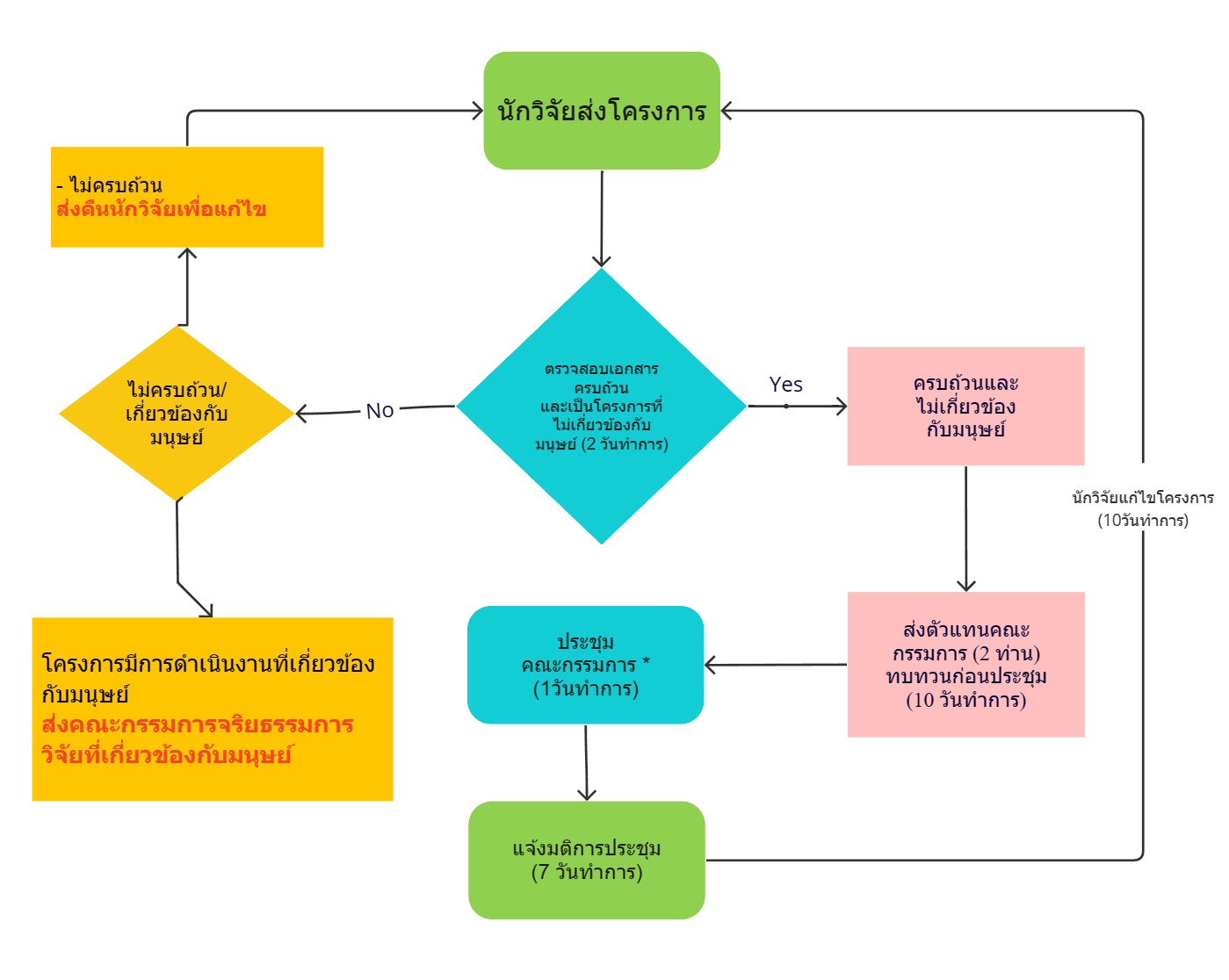
ขั้นตอนการส่งโครงการวิจัยครั้งแรก (Initial Submission)
ตารางการประชุมประจำปีงบประมาณ พ.ศ.2567
กำหนดวันประชุมอย่างน้อยเดือนละ 1 ครั้ง
ภาพกระบวนการ
เนื่องจากในสถานการณ์ปัจจุบันยังไม่มีการประกาศให้โรคใดเป็นภาวะฉุกเฉินทางสาธารณสุข ดังนั้น จึง "ยังไม่เปิดรับพิจารณาโครงการ" ในขณะนี้
- LC01_แบบบันทึกข้อความส่งโครงการ
- การวิจัยที่เกี่ยวข้องกับมนุษย์ (จำนวน 13 ชุด)
- 1.1 แบบตรวจสอบความครบถ้วนของ หัวข้อต่างๆ ในแบบเสนอโครงการวิจัย 1 ชุด
- 1.2 แบบเสนอโครงการวิจัย**ไม่ต้องเข้ารูปเล่ม**
- 1.3 เอกสารแนะนำสำหรับอาสาสมัครและใบยินยอมเข้าร่วมโครงการของอาสาสมัคร **จำนวนเอกสารต้องส่งตามจำนวนโครงร่างวิจัย**
- ♦ information sheet
- ♦ consent form
- ♦ information sheet 7-12 years
- ♦ consent form 7-12 years
- ♦ consent form parents & legally authorized representative (LAR)
- 1.4 กรณีที่ผู้วิจัยได้รับมติให้ปรับปรุงแก้ไขโครงร่างการวิจัย กรุณาส่งแบบสรุปประเด็นที่แก้ไขตามมติกรรมการ
- 1.1 แบบตรวจสอบความครบถ้วนของ หัวข้อต่างๆ ในแบบเสนอโครงการวิจัย 1 ชุด
- 1.2 แบบเสนอโครงการวิจัย**ไม่ต้องเข้ารูปเล่ม**
- 1.3 เอกสารแนะนำสำหรับอาสาสมัครและใบยินยอมเข้าร่วมโครงการของอาสาสมัคร **จำนวนเอกสารต้องส่งตามจำนวนโครงร่างวิจัย**
- ♦ information sheet
- ♦ consent form
- ♦ information sheet 7-12 years
- ♦ consent form 7-12 years
- ♦ consent form parents & legally authorized representative (LAR)
- 1.4 กรณีที่ผู้วิจัยได้รับมติให้ปรับปรุงแก้ไขโครงร่างการวิจัย กรุณาส่งแบบสรุปประเด็นที่แก้ไขตามมติกรรมการ
- ♦ แบบเสนอขอแก้ไขในโครงร่างการวิจัย (Protocol Amendment)
- ♦ สำเนาโครงร่างวิจัยที่ได้รับการรับรองฉบับล่าสุด
- ♦ โครงร่างวิจัยที่มีการเปลี่ยนแปลง (ทำ Highlight ส่วนที่มีการแก้ไข) 2.2 การรายงานไม่ปฏิบัติตามโครงร่างการวิจัย
- ♦ สำเนาโครงร่างวิจัยที่ได้รับการรับรองฉบับล่าสุด
- ♦ แบบรายงานการไม่ปฏิบัติตามโครงร่างการวิจัยที่ได้รับรอง (Protocal non - compliance Report) 2.3 รายงานเหตุการณ์ไม่พึงประสงค์จากการวิจัย (Adverse Event Report)
- ♦ สำเนาโครงร่างวิจัยที่ได้รับการรับรองฉบับล่าสุด
- ♦ แบบรายงานเหตุการณ์ไม่พึงประสงค์จากการวิจัย (Adverse Event Report) 2.4 การขอต่ออายุโครงร่างวิจัย/ ขยายเวลาโครงร่างวิจัย
- ♦ สำเนาโครงร่างวิจัยที่ได้รับการรับรองฉบับล่าสุด
- ♦ แบบรายงานความก้าวหน้าของการวิจัย 2.5 การแจ้งยุติโครงการวิจัยก่อนกำหนด
- ♦ สำเนาโครงร่างวิจัยที่ได้รับการรับรองฉบับล่าสุด
- ♦ แบบรายงานการยุติโครงการวิจัยก่อนกำหนด (Premature termination) 2.6 การแจ้งปิดโครงการวิจัย (เมื่อดำเนินการวิเคราะห์ข้อมูลเสร็จสิ้น)
- ♦ สำเนาโครงร่างวิจัยที่ได้รับการรับรองฉบับล่าสุด
- ♦ แบบรายงานเสร็จสิ้นโครงการวิจัย(Final Report)
- ♦ แบบเสนอขอแก้ไขในโครงร่างการวิจัย (Protocol Amendment)
- ♦ สำเนาโครงร่างวิจัยที่ได้รับการรับรองฉบับล่าสุด
- ♦ โครงร่างวิจัยที่มีการเปลี่ยนแปลง (ทำ Highlight ส่วนที่มีการแก้ไข) 2.2 การรายงานไม่ปฏิบัติตามโครงร่างการวิจัย
- ♦ สำเนาโครงร่างวิจัยที่ได้รับการรับรองฉบับล่าสุด
- ♦ แบบรายงานการไม่ปฏิบัติตามโครงร่างการวิจัยที่ได้รับรอง (Protocal non - compliance Report) 2.3 รายงานเหตุการณ์ไม่พึงประสงค์จากการวิจัย (Adverse Event Report)
- ♦ สำเนาโครงร่างวิจัยที่ได้รับการรับรองฉบับล่าสุด
- ♦ แบบรายงานเหตุการณ์ไม่พึงประสงค์จากการวิจัย (Adverse Event Report) 2.4 การขอต่ออายุโครงร่างวิจัย/ ขยายเวลาโครงร่างวิจัย
- ♦ สำเนาโครงร่างวิจัยที่ได้รับการรับรองฉบับล่าสุด
- ♦ แบบรายงานความก้าวหน้าของการวิจัย 2.5 การแจ้งยุติโครงการวิจัยก่อนกำหนด
- ♦ สำเนาโครงร่างวิจัยที่ได้รับการรับรองฉบับล่าสุด
- ♦ แบบรายงานการยุติโครงการวิจัยก่อนกำหนด (Premature termination) 2.6 การแจ้งปิดโครงการวิจัย (เมื่อดำเนินการวิเคราะห์ข้อมูลเสร็จสิ้น)
- ♦ สำเนาโครงร่างวิจัยที่ได้รับการรับรองฉบับล่าสุด
- ♦ แบบรายงานเสร็จสิ้นโครงการวิจัย (Final Report)
กรณี อาสาสมัครอายุ 18 ปีขึ้นไป
กรณี อาสาสมัครอายุต่ำกว่า 18 ปี
กรณี อาสาสมัครอายุ 18 ปีขึ้นไป
กรณี อาสาสมัครอายุต่ำกว่า 18 ปี
(ดำเนินการก่อนหนังสือรับรองหมดอายุ ล่วงหน้า 2 เดือน)
(ดำเนินการก่อนหนังสือรับรองหมดอายุ ล่วงหน้า 2 เดือน)
- ♦ บางโครงการอาจได้รับการตรวจเยี่ยม (Inspection) จากคณะกรรมการฯ ตามเงื่อนไขที่กำหนดระหว่างการดำเนินการวิจัย
- ♦ คลินิกจริยธรรมการวิจัย (ผู้วิจัยสามารถประสานขอวัน หรือนัดหมายผ่านทางสำนักงานเลขานุการฯ)
- สำนักงานเลขานุการคณะกรรมการจริยธรรมการวิจัย
- กรมควบคุมโรค กองนวัตกรรมและวิจัย
- อาคาร 10 ชั้น 1 ถนนติวานนท์ ต.ตลาดขวัญ อ.เมือง จ.นนทบุรี 11000
- โทรศัพท์ 02-5903149, 062-553-0068
- E-mail: [email protected]
- ฝ่ายเลขานุการ คณะกรรมการจริยธรรมการวิจัย กรมควบคุมโรค
- นางสาวอรวี ลี้เกษร
- นางสาวสุนิสา ปานสอาด
- นางสาวกัญญาณัฐ บุญเข็ม
- นางสาวสุรัสวดี กลิ่นชั้น